Укажите ряд, в котором приведены формулы двух сложных и одного простого вещества:
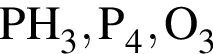
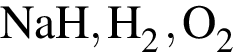
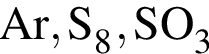
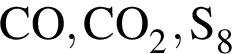
Укажите ряд, в котором приведены формулы двух сложных и одного простого вещества:
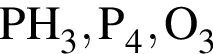
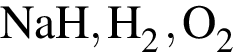
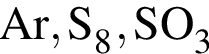
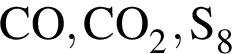
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 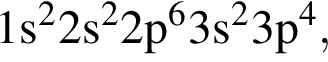 находится в группе:
находится в группе:
Высшему оксиду элемента, порядковый номер которого 33, соответствует гидроксид состава:

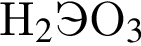

Все порции вещества, формула которого H2S содержится 1 моль атомов серы. Укажите объем (дм3) порции при н. у.:
Установите соответствие между формулой вещества и степенью окисления в нем атома химического элемента,указанного в скoбках.
1) Al4C3(C)
2) H2O2(O)
3) KHSO3(S)
a) –1
б) –2
в) –4
г) +4
д) +6
Степень окисления –1 имеют атомы одного из элементов в соединении:
Основная соль может образоваться при взаимодействии азотной кислоты с каждым из гидроксидов, названия которых:
Как кислотными, так и основными свойствами обладает каждый из оксидов ряда:
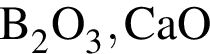
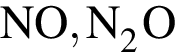
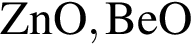
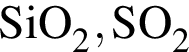
Каолинит — основной компонент глин — является природным:
Укажите верное утверждение:
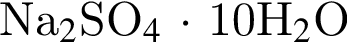 является кислой солью
является кислой солью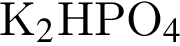 относится к сильным электролитам
относится к сильным электролитам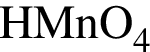 образует как средние, так и кислые соли
образует как средние, так и кислые солиСогласно положению в периодической системе в порядке усиления неметаллических свойств элементы расположены в ряду:
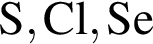
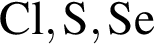
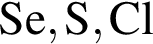
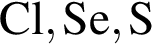
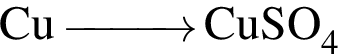
Используя в качестве реагента только разбавленную серную кислоту, в одну стадию можно осуществить превращение:
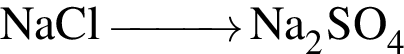


Бром, так же как и йод:
а) образует галогениды
б) является жидкостью (н. у.)
в) НЕ имеет аллотропных модификаций
г) образует сильную галогеноводородную кислоту
Реагируют с концентрированной серной кислотой, но НЕ реагируют с разбавленной серной кислотой оба вещества пары:
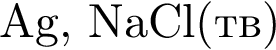
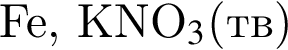
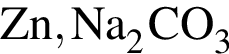
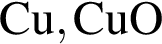
Разбавленная фосфорная кислота вступает в реакции соединения с веществами:
a — 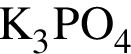
б — ![]()
в — ![]()
г — ![]()
Очистить угарный газ от углекислого можно с помощью водных растворов веществ:
а — 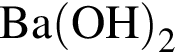
б — 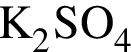
в — 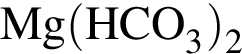
г — 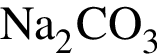
Выберите правильное утверждение:
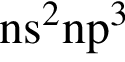
Укажите схемы процессов окисления:
а) 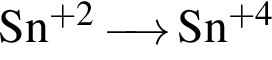
б) 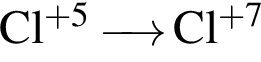
в) 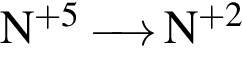
г) 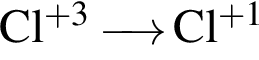
В отличие от воды разбавленный водный раствор гидроксида калия растворяет:
а) ![]()
б) ![]()
в) ![]()
г) ![]()
В замкнутой системе протекает реакция между газообразными веществами

Укажите все факторы, увеличивающие скорость прямой реакции:
а — понижение давления в системе
б — повышение температуры
в — увеличение концентрации вещества А
г — увеличение объема системы
В закрытом сосуде протекает химическая реакция А + 3В = 3С + D. До начала реакции молярная концентрация вещества А равнялась 1 моль/дм3, а вещества С — 0 моль/дм3. Через сколько секунд концентрации веществ А и С сравняются, если скорость образования вещества С составляет 0,03 моль/дм3 · с (все вещества — газы, объем сосуда постоянный)?
Число возможных попарных взаимодействий в разбавленном водном растворе между ионами 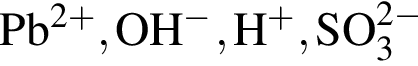 равно:
равно:
В водном растворе в значительных количествах совместно могут находиться ионы пары:
К увеличению ![]() водного раствора приведет:
водного раствора приведет:
Для подкормки растений на 1 м2 почвы необходимо внести азот массой 5,6 г и калий массой 11,7 г. Укажите массу (г) смеси, состоящей из аммиачной и калийной селитры, которая потребуется, чтобы растения получили необходимое количество азота и калия на поле площадью 100 м2.
Укажите общие свойства для бериллия и кальция:
а) растворяются в водных растворах щелочей, образуя комплексные соли
б) электронная конфигурация внешнего энергетического уровня в основном состоянии — ![]()
в) с водой реагируют при комнатной температуре
г) гидроксиды реагируют с кислотами
Назовите по систематической номенклатуре соединение, формула которого:
Аминоуксусная кислота взаимодействует с веществами, формулы которых (электролиты взяты в виде водных растворов):
а) ![]()
б) ![]()
в) ![]()
г) ![]()
Выберите утверждения, справедливые для этанола:
1) является гомологом вещества, формула которого
2) температура кипения выше, чем у этана
3) при взаимодействии с натрием образуются вещества, формулы которых 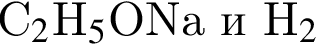
4) при взаимодействии с уксусной кислотой в присутствии серной кислоты образует соединение, формула которого
5) при взаимодействии с бромоводородом образуется бромэтан и выделяется водород
6) образуется при окислении уксусного альдегида
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 135.
В результате гидролиза сахарозы в присутствии разбавленной серной кислоты был получен раствор с массовой долей сахарозы 4 %. Рассчитайте массовую долю (%) глюкозы в полученном растворе, если в реакцию гидролиза вступило 70 % сахарозы. Ответ округлите до целых.
Смесь алканов подвергли пиролизу. В результате образовалась смесь этена, пропена и водорода с массовой долей водорода 1,80%. Вычислите молярную массу (г/моль) исходной смести алканов.
Соль А, известная под названием растворимое стекло, образована металлом группы IA. При пропускании избытка углекислого газа через водный раствор A образуется соль Б и плохо растворимая в воде кислота В. При нагревании В разлагается на воду и оксид Г. Сплавление Г с содой приводит к образованию исходной соли А и не имеющего запаха газообразного вещества Д. Найдите сумму молярных масс(г/моль) веществ Б, Г, Д.
K раствору сульфата меди(II) массой 600 г с массовой долей 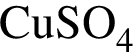 4% добавили медный купорос массой 55 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.
4% добавили медный купорос массой 55 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.
Дана схема превращений
Вычислите сумму молярных масс (г/моль) твёрдого при температура 20 °C неорганического вещества ![]() и органического вещества молекулярного строения
и органического вещества молекулярного строения ![]()
Под плодовые деревья необходимо внести 77,0 г азота и 131,6 г оксида калия ![]() . Укажите суммарную массу (г) аммиачной селитры
. Укажите суммарную массу (г) аммиачной селитры 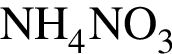 и калийной селитры
и калийной селитры ![]() , которые потребуются, чтобы деревья получили необходимые количества азота и калия.
, которые потребуются, чтобы деревья получили необходимые количества азота и калия.
К раствору серной кислоты массой 224 г добавит смесь нитратов бария и свинца(II). За счет протекания реакции масса раствора увеличилась на 4,2 г, а массовые доли кислот в растворе уравнялись. Вычислите массовую долю (%) серной кислоты в исходном растворе.
В результате полного восстановления оксида меди(II) углеродом была получена смесь угарного и углекислого газов количеством 1,7 моль и массой 63,6 г. Рассчитайте массу (г) образовавшейся при этом меди.
При полном сгорании метана химическим количеством 1 моль в кислороде выделяется 890 кДж теплоты, а в озоне — 1032 кДж. В результате сгорания смеси объемом (н. у.) 35,392 дм3, состоящей из метана и озонированного кислорода (смесь озона с кислородом), газы прореагировали полностью с образованием углекислого газа и воды. Определите количество теплоты (кДж), выделившейся при этом, если доля озона в озонированном кислороде составляет 32% по объему.
К 40 дм3 смеси, состоящей из этана и аммиака, добавили 15 дм3 хлороводорода. После приведения новой газовой смеси к первоначальным условиям её относительная плотность по воздуху составила 0,90. Укажите массовую долю (%) аммиака в исходной смеси. (Все объемы измеряли при t = 20 °C, Р = 105 Па.)
Загрязненный аммиак объемом 32 м3 (н. у.) содержит 10% примесей (по объему). В результате поглощения всего аммиака избытком азотной кислоты была получена аммиачная селитра. Учитывая, что для подкормки одного плодового дерева необходимо 45 г химического элемента азота, рассчитайте, какое количество деревьев можно подкормить, используя полученную селитру.
Тепловой эффект реакции образования карбоната кальция из оксидов составляет 178 кДж/моль. Для полного разложения некоторого количества карбоната кальция потребовалось 64,08 кДж теплоты. Полученный оксид кальция спекали с углем массой 18 г в электропечи. Вычислите массу (г) образовавшегося при этом бинарного соединения, в котором массовая доля кальция равна 62,5%. (Примесями пренебречь.)
Электролиз водного раствора, содержащего хлорид калия массой 268,2 г, протекает по схеме
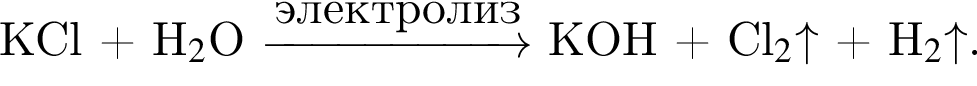
Рассчитайте объем (н. у., дм3) выделившегося в результате реакции хлора, если его выход составляет 60%.
Порцию кристаллогидрата соли 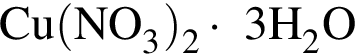 прокалили. Образовался черный порошок, а остальные продукты реакции были полностью поглощены водой. Образовавшийся раствор сильной кислоты объемом 3 дм3 имеет
прокалили. Образовался черный порошок, а остальные продукты реакции были полностью поглощены водой. Образовавшийся раствор сильной кислоты объемом 3 дм3 имеет ![]() Рассчитайте массу (г) черного порошка.
Рассчитайте массу (г) черного порошка.